RS1000DI Портативний раманівський ідентифікатор RS1500DI
★ Можна ідентифікувати широкий спектр хімічної, біохімічної сировини та пігментів
★ Його можна перевірити безпосередньо через скло, плетені мішки, паперові пакети, пластик та інше пакування (RS1500DI)
★ Маленький і легкий, його можна гнучко переміщувати на складах, у приміщеннях для підготовки матеріалів, виробничих цехах та інших місцях
★ Швидка відповідь і ідентифікація можуть бути завершені за секунди
★ Немає необхідності брати проби, немає необхідності переносити сировину та допоміжні матеріали до кімнати для відбору, що може уникнути забруднення зразків
★ Точна ідентифікація, використання розширеного алгоритму машинного навчання, сильна специфічність
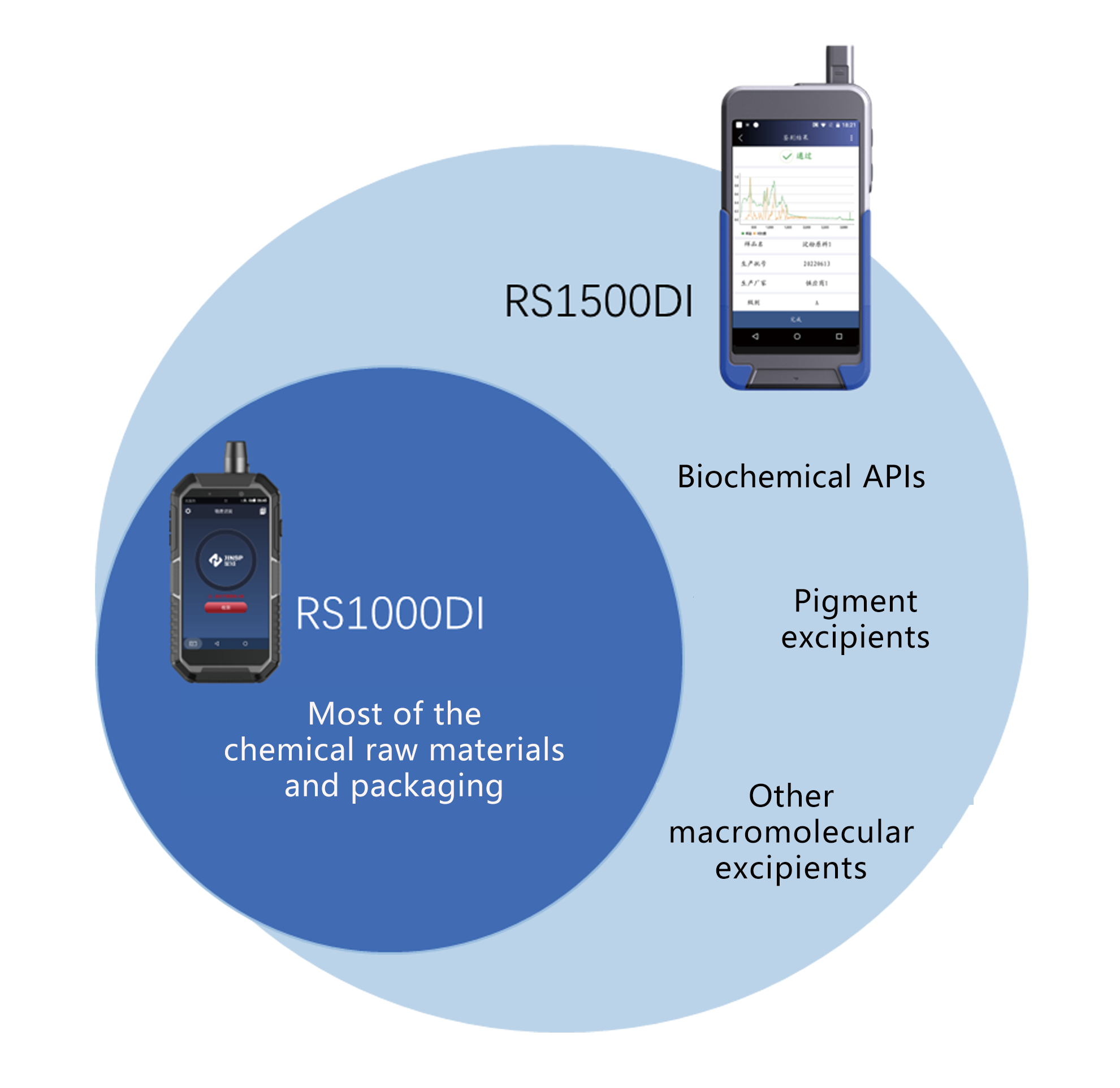
RS1000DI & RS1500DI
• Хімічна сировина: аспірин, ацетамінофен, фолієва кислота, ніацинамід та ін.
• Фармацевтичні допоміжні речовини: солі, луги, цукри, естери, спирти, феноли та ін.
• Пакувальний матеріал: поліетилен, поліпропілен, полікарбонат, етилен-вінілацетатний сополімер
RS1500DI
• Біохімічні АФІ: амінокислоти та їх похідні, ферменти та коферменти, білки
• Допоміжні речовини пігменту: кармін, каротин, куркумін, хлорофіл та ін.
• Інші високомолекулярні допоміжні речовини: желатин, целюлоза мікрокристалічна та ін.
RS1500DI:
| Специфікація | опис |
| технології | Раманівська технологія |
| Laser | 1064 нм |
| Wвісім | 730 г (з акумулятором) |
| Cпідключення | USB/ Wi-Fi/ 4G/ Bluetooth |
| Pвласник | Літій-іонний акумулятор |
| Dформат ata | SPC/ txt/ JEPG/ PDF |
RS1000DI:
| Специфікація | опис |
| Лазерна | 785 нм |
| вага | <500 г (включаючи акумулятор) |
| Підключення | USB/ Wi-Fi/ 4G/ Bluetooth |
| потужність | Літій-іонний акумулятор |
| Формат даних | SPC/ txt/ JEPG/ PDF |
1. Програма співробітництва міжнародної фармацевтичної інспекції (PIC/S) та її Керівні принципи GMP:
Додаток 8 Відбір зразків сировини та пакувальних матеріалів Ідентифікація всієї партії матеріалів може бути підтверджена лише після проведення тесту на ідентифікацію зразків у кожному пакувальному контейнері.
2. Поточна належна виробнича практика US FDA GMP:
FDA 21 CFR, частина 11: для кожного компонента лікарського засобу необхідно провести принаймні один ідентифікаційний тест;
Інструкція інспектора FDA: Проведіть принаймні один спеціальний ідентифікаційний тест для кожної партії кожної сировини.











